医疗器械飞行检查与技术转让 法规框架与实施要点
医疗器械作为保障公众健康的重要产品,其安全性与有效性至关重要。为了确保医疗器械全生命周期的合规性,监管部门采取了多种监管措施,其中“飞行检查”与“技术转让”是两个关键环节。本文将系统介绍医疗器械领域的飞行检查,并探讨其在技术转让过程中的特殊意义与实施要点。
一、 医疗器械飞行检查概述
飞行检查,又称“不预先通知的检查”,是指药品监督管理部门根据监管需要,对医疗器械研制、生产、经营和使用等环节开展的不事先告知的现场监督检查。其核心特点是突击性和随机性,旨在真实反映企业日常质量管理体系的运行状况。
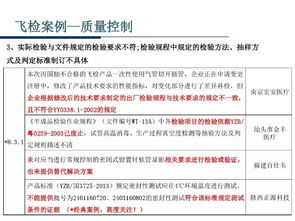
- 检查依据与目的:主要依据《医疗器械监督管理条例》、《医疗器械生产质量管理规范》(GMP)及相关附录等法规文件。目的是发现和防控风险,震慑违法违规行为,督促医疗器械相关企业持续符合法定要求。
- 检查重点:通常聚焦于质量管理体系的关键要素,如机构与人员、厂房与设施、设备管理、文件管理、设计开发、采购、生产管理、质量控制、销售与售后服务、不合格品控制、不良事件监测与报告等。对于有不良记录、投诉举报多、风险等级高的产品和企业,更是飞行检查的重点关注对象。
- 检查结果与处理:检查中发现的问题将形成书面记录,严重的可能面临限期整改、停产整顿、召回产品甚至吊销许可证书等处理措施。检查结果通常会向社会公开,对企业的声誉和市场活动产生直接影响。
二、 技术转让中的特殊考量
技术转让是指将医疗器械产品的生产技术、质量管理体系、相关知识产权及文件等,从一个场地(转让方)转移到另一个场地(受让方)的过程。这在新产品引入、企业并购、产能调整等场景中常见。在此过程中,飞行检查的风险显著增加,因为体系处于变动和磨合期。
- 转让过程本身是监管焦点:监管部门会密切关注技术转让是否可能导致产品质量波动或体系管理脱节。因此,技术转让活动本身就可能触发针对性的飞行检查,以评估转让的合规性与完整性。
- 飞行检查的重点转移:在技术转让背景下,飞行检查不仅关注常规GMP符合性,还会特别审视:
- 技术转移的充分性与有效性:验证方案是否科学,知识转移是否完整,人员培训是否到位,工艺验证是否充分。
- 体系的衔接与融合:受让方的质量管理体系是否能无缝承接转让方的要求,文件系统是否已更新并有效执行。
- 变更管理的合规性:涉及场地、工艺、设备等重大变更是否按规定进行了充分的评估、验证和申报。
- 首批产品的质量:对技术转让后生产的前几批产品,其质量数据、稳定性考察及放行控制会成为检查重点。
三、 应对策略与最佳实践
为平稳度过技术转让期并有效应对潜在的飞行检查,相关企业应采取以下策略:
- 前期充分准备:在转让计划阶段就进行差距分析,识别法规和标准要求上的差异。制定详细、可行的技术转移方案,明确时间表、责任人与交付物。
- 建立联合质量团队:转让方和受让方应组建联合工作组,确保沟通顺畅,确保所有关键技术、诀窍(Know-how)和质量管理要求被清晰理解、准确转移和记录。
- 进行全面验证:严格执行工艺验证、清洁验证、分析方法转移等,用数据证明在受让场地能持续稳定生产出符合预定标准的产品。
- 完善文件体系:及时修订或新建所有相关质量文件,包括质量标准、工艺规程、SOP(标准操作规程)等,并确保相关人员已接受培训并能严格执行。
- 模拟审计与自查:在技术转移完成后、正式商业化生产前,建议进行多次内部模拟审计或邀请第三方审计,主动发现和纠正问题,使体系达到稳定运行状态。
- 保持透明沟通:对于涉及注册证变更的技术转让,应主动与监管部门沟通进展,按时提交相关变更资料,避免因信息不畅引发监管关注。
结论
医疗器械的飞行检查是保障产品安全有效的利剑,而技术转让则是产业发展的常见活动。将飞行检查的严格标准内化于技术转让的全过程管理之中,是企业规避风险、确保合规运营的明智之举。通过周密规划、扎实执行和持续改进,企业不仅能够成功实现技术转移,更能借此机会提升整体质量管理水平,在日益严格的监管环境下赢得竞争优势。
如若转载,请注明出处:http://www.eeqldln.com/product/75.html
更新时间:2026-05-31 13:52:29